Трис является широко используемой буферной системой в биохимических экспериментах и биологических препаратах, которая широко используется в биомедицине и других областях. Команда AVT представит вам коммерчески доступный конъюгат антитело-лекарственное средство (ADC), в котором используется трис в составе, иноузумаб озогамицин (Besponsa), который разработан Pfizer.
Его формулировка заключается в следующем:
Ингредиент | Иноузумаб озогамицин | Полисорбат 80 | Накл | Сахароза | Трометамин (ТРИС) | Вода для инъекций | РН |
Содержание | 0,9 мг | 0,36 мг | 2,16 мг | 180 мг | 8,64 мг | 4 мл | Около 8,0 |
Озогамицин Inotuzumab (Besponsa) представляет собой инновационный ADC, разработанный Pfizer, состоящий из моноклонального антитела, нацеленного на CD22, и цитотоксического агента калихеамицина. Беспонса®Коммерчески доступен в лиофилизированном порошке, в котором,Сахароза для продажиГлавным образом действует как криопротектант и трометамин (ТРИС) буфер пэ-аш.
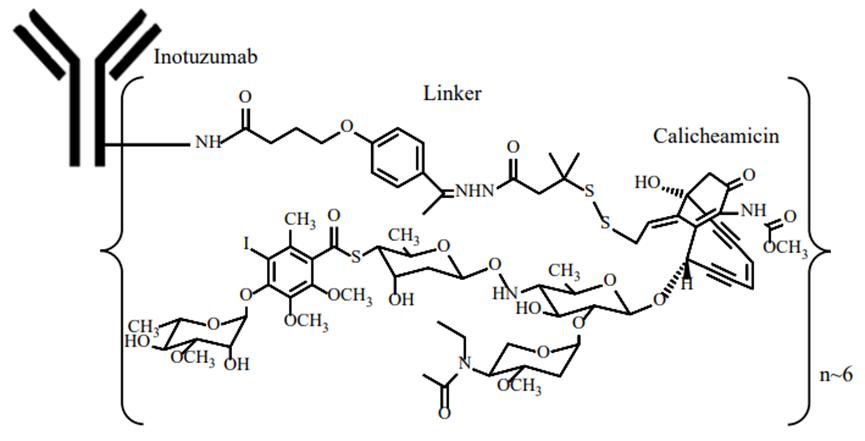
Озогамицин Inotuzumab способен воздействовать на раковые клетки и связываться с антигеном CD22, который повсеместно присутствует на поверхности В-клеток. Впоследствии эти АЦП будут эндоцитозироваться в раковые клетки, а азитромицин будет в дальнейшем проявлять свою эффективность и вызывать гибель раковых клеток. Эти АЦП будут затем эндоцитозированы в раковые клетки, где калихеамицин будет дополнительно убивать раковые клетки.
28 июня 2017 года BESPONSA была одобрена для маркетинга в ЕС.
Трис USP оптомИспользуется в производстве Besponsa, который получил одобрение Управления по контролю за продуктами и лекарствами США (FDA) 17 августа 2017 года. Этот препарат специально разработан для лечения рецидива или рефрактерного предшественника B-клеточного острого лимфобластного лейкоза (ALL) у взрослых.Примечательно, что Беспонса является первым одобренным FDA конъюгатом антитело-лекарственное средство (ADC), нацеленным на CD22.
22 декабря 2021 года Inotuzumab Ozogamicin for Injection (Besponsa), АЦП CD22, разработанный Pfizer, был официально одобрен для маркетинга в Китае для взрослых пациентов с рецидивирующим или рефрактерным предшественником В-клеточного острого лимфобластного лейкоза (ВСЕ).Как 4ThADC одобрен для маркетинга в Китае.